SLA et cancer
Il existe un mystère persistant sur les mécanismes causatifs de la SLA. Les travaux intenses depuis deux décennies, sur la SOD1 n’ont pas aidé à comprendre de manière concluante son lien avec la maladie. De nombreuses mutations de SOD1 produisent des phénotypes de SLA très similaires. Mais ces mutations n'ont pas empêché les neurones de fonctionner correctement pendant plusieurs décennies, de sorte qu'il est difficile de les invoquer pour expliquer l'apparition de la maladie. Même s'il y a moins de travaux scientifique concernant FUS ou TDP-43, car leur découverte est plus récente, le mystère est également complet sur la manière dont une protéine TDP-43 non mutée et mal localisée dans le cytoplasme, pourrait tuer un neurone. Le seul cas évident est celui de C9orf72, où les répétions de dipeptide, ne pourrait manifestement pas produire de protéine fonctionnelle. Cependant même dans ce cas, on ignore pourquoi la SLA se déclare seulement à un âge avancé.
PARP est impliqué dans la réparation de l'ADN
Il y a un lien troublant entre le cancer et la SLA, par exemple il y a une relation inverse entre l'apparition du cancer et l'apparition de la SLA. Les médicaments contre la SLA ont également des propriétés anticancéreuses. Donc, il n’est peut-être pas surprenant qu’ils puissent partager une cause fondamentale: des défauts dans les mécanismes de réparation de l’ADN. Les poly-ADP-ribose polymérases (PARP) interviennent dans la réparation de l'ADN, tout comme FUS ou TDP-43.
Lors de dommages à l'ADN ou de stress cellulaire, les PARP sont activés, entraînant une augmentation de la quantité de poly-ADP-ribose et une diminution de la quantité de NAD+.
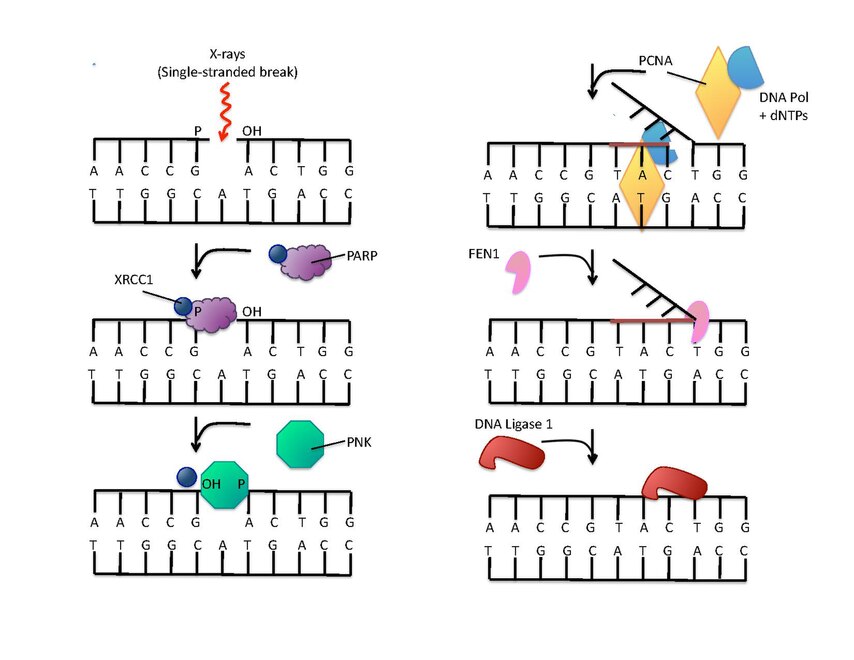
La mauvaise localisation de FUS et TDP-43 dans le cytoplasme inhibe le mécanisme de réparation de l’ADN
FUS et TDP-43 jouent tous deux un rôle dans le traitement de l'ARN, y compris l'épissage, la transcription et le transport. L'implication de FUS et de TDP-43 dans la réponse aux dommages du génome cellulaire a été découverte récemment. Dans les neurones sains, le FUS protège le génome en facilitant le recrutement dépendant de PARP-1. Les auteurs rapportent que TDP-43 est un composant essentiel de la voie de réparation de rupture d'ADN à double brin (ADN) médiée par une jonction d'extrémité (NHEJ). TDP-43 est rapidement recruté sur les sites d'ADN à double brin pour interagir de manière stable avec les facteurs DDR et NHEJ, agissant en particulier comme un échafaudage pour le recrutement du complexe XRCC4-ADN ligase 4 isolant aux sites DSB. En effet, la présence de fragmentation de TDP-43 et son agrégation dans des échantillons de SLA est fortement corrélées à la présence de PARP-1 et de caspase-3 clivées.
Au cours de l'apoptose, la PARP se déplace vers le cytoplasme
Les caspases sont une famille de protéases de la cystéine qui jouent un rôle essentiel dans la mort cellulaire programmée. Cette protéase clive PARP-1 en deux fragments, la laissant complètement inactive, afin de limiter la production de poly-ADP-ribose. L'un de ses fragments migre du noyau vers le cytoplasme et est considéré comme une cible de l'auto-immunité. Au début de l'année 2019, il a été constaté qu'une dysrégulation de la PARylation pourrait contribuer à la pathogenèse de la SLA en favorisant l'agrégation des protéines.
Bien que la PARylation se produise principalement sur les protéines PARP, l'association de la PAR aux granules liées à la SLA a été observée.
Chaine causale de la SLA
Les résultats des scientifiques relient donc la pathologie de TDP-43 à une réparation altérée du DSB et à une signalisation persistante du DDR dans les maladies du motoneurone, et suggèrent que les thérapies ciblées sur la réparation du double brin d'ADN, pourraient améliorer l'instabilité du génome induite par la toxicité du TDP-43 dans les maladies du motoneurone.
En résumé:
- Des mutations de FUS ou de TDP-43 rendraient inefficace la réparation de l'ADN.
- L'intervention de PARP réparerait cet ADN et transfèrerait TDP-43 dans des granules localisés dans le cytoplasme.
- Cela aggraverait encore les problèmes de réparation de l'ADN.
Un possible méchanisme thérapeutique
Ces nouvelles découvertes permettent de mieux comprendre comment un défaut de réparation de l’ADN peut être associé à la neurodégénérescence FUS et/ou TDP-43, et soulève la question de savoir si la résolution des problèmes de ligature de l’ADN serait une voie prometteuse pour la mise au point de traitements neuroprotecteurs.

